Bleiakkus
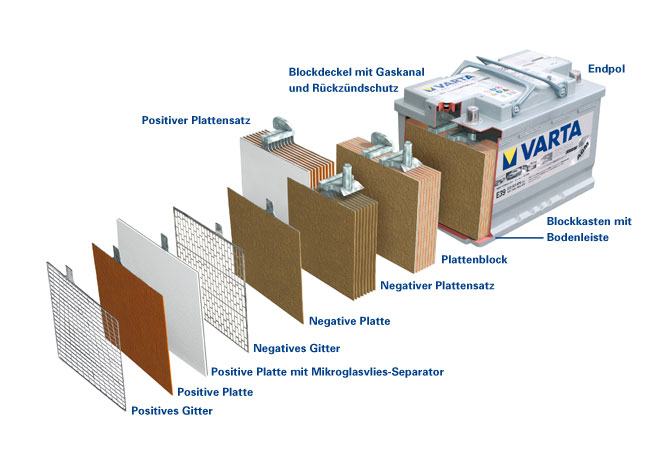
Aufbau
- Stromableiter bestehen aus Reinblei oder Bleilegierungen
- Aufbau meist als Gitterplatte oder Panzerplatte
- Reinblei ist weich, und kann deswegen nur in gewicktlten Zellen verwendet werden. Der Vorteil ist die gute Korrosionsbeständigkeit. Allerdings kann an der positiven Elektrode eine Passivierungsschicht entstehen, welche den Kontakt zum Aktivmaterial verschlechtert. Die Zyklenfestigkeit des Positiven Gitters ist sehr schlecht.
- Bleilegierungen
- Blei-Antimon: erhöhung der mechanischen Stabilität, verbesserung der Zyklenlebensdauer, höherer Wasserverbrauche, nicht für verschlossene Batterien geeignet.
- Blei-Zinn: Verbessert die Eigenschaften als positives Gitter. Ladbarkeit nimmt zu, Korrosion und Passivierung wurd reduziert. Ab 0.8% Zinn nimmt die Korrosion wieder zu.
- Blei-Calcium-Zinn: Calcium hat nur in der Produktion einen Vorteil, da die Legierung beim Gießen schneller aushärtet. Calcium verschlechtert allerdings die Korrosionseigenschaften, was durch Zugabe von etwa 1.2% Zinn wieder ausgeglichen wird.
- Negative Elektrode (Anode) besteht aus Blei
- zur erhöhung der Leitfähigkeit wir das Aktivmaterial mit bis zu 3% Kohlenstoff versetzt.
Additive (Lignin) zur erhöhung der Porösität und stabilisierung der porösen Struktur bei der Zyklisierung -> Expander
- Positive Elektrode (Kathode) besteht aus Bleidioxid
- zumischung von Fasern die für die poröse Struktur sorgen.
- Elektrolyt ist verdünnte Schwefelsäure
- Das Elektrolyt ist an der Hauptreaktion beteiligt, deswegen ändert sich die Konzentration mit dem Ladestand.
- Die Säurekonzentration ist mit geringem Ladestand kleiner, was den Gefrierpunkt angebt und die Kaltstarteigenschaften verschlechtert.
- Die Benötigte Menge an Elektrolyt ist durch die Bleikapazität festgelegt.
- bei verschlossen Akkus wird das Elektrolyt in Vlies oder Gel gebunden.
- Gaskanäle gewährleisten den Sauerstoffkreislauf.
- Separator
- hohe Ionenleitfähigkeit
feine Poren um das Wachstum von Dentriten (Metallische Auswüchse die zu Kurzschlüssen führen könne) zu hemmen.
Reaktionenn
Lade- / Entladereaktion
Entladereaktionen Negativer Pol:
Pb + SO42- -> PbSO4 + 2e-
Positiver Pol:
PbO2 + SO42- + 4 H3O+ + 2e- -> PbSO4 + 6H2O
Beim Laden laufen die Vorgänge in Gegenrichtung ab.
Die Gesamtreaktion:
Pb + PbO2 + 2H2SO4 -> 2PbSO4 + 2H2O + elektrische Energie
Nach rechts findet unter Energieabgabe die Entladung des Bleiakkus statt, nach links unter Energiezufuhr die Aufladung.
Aus der elektrochemischen Spannungsreihe kann man nun die Potentialdifferenz, also letztlich die elektrische Spannung, die entsteht, berechnen.
Pb + SO42- -> PbSO4 + 2e- | -0,36V PbO2 + SO42- + 4H3O+ + 2e- -> PbSO4 + 6H2O | +1,67V E0Ges = 1,68V - (-0,36V) = 2,04V
Selbstentladung:
2PbO2 + 2H2SO4 -> 2PbSO4 + 2H2O + O2
Alterung
Mechanismus |
Beschreibung |
Folge |
Ursachen |
Korrosion des positiven Ableiters |
durch eletrochemische oxidation beim Laden und der Wechselwirkung zwischen Ableiter und Aktivmaterial korrodiert das Ableiter-Gitter. |
- ohmscher Widerstand nimmt zu |
- hohe Ladesannung |
Erweichung der Aktivmasse |
Durch mechanischen Stress in der Aktivmasse kommt es zum Verlust an elektrischer und mechanischer Kontaktierung |
- Ausfall der Aktivmasse |
- mechanischer Stress beim Zyklisieren |
Sulfation der positiven und negativen Platte |
Es bilden sich große Bleisulfatkristalle die sich auch durch längeres Laden nicht mehr umwandeln lassen |
- Kapazitätsverlust |
- lange Standzeiten |
Verbleiung der positiven und negativen Platte |
Verlust der Expander in der negativen Aktivmasse; dadurch verdichtet sich das aktive Material, die zur Verfügung stehende Oberfläche verringert sich. |
Veringerung der Kapazität |
- hoher Ladungsdurchsatz |
Gitterwachstum |
Die Korrosionsprodukte nehmen größeres Volumen als die Ausgangsprodukte ein. |
kurzschluss zwischen den Platten |
- Alle Ursachen der Korrosion |
Dentritenwachstum |
Dentriten enstehen immer dann, wenn nicht genug Kristallisationskeime zur Verfügung stehen oder wenn die Löslichkeit von Bleisulfat sehr hoch ist. |
- kurzschluss zwischen den Platten |
- hohe Stromdichte beim Entladen |
zerstörung des Separators |
durch die mechanische beanspruchung und die zersetzung des Separators erfolgt dessen Zersetzung. |
Kurzschluss |
- Gitterwachstum |
Optimaler Betrieb von Bleiakkus
Zur Erzielung möglichst langer Lebensdauern ist folgendes zu beachten:
- Bleibatterien dürfen nur so tief wie nötg entladen werden.
Vor dem Laden sollten Bleibatterien nicht erst vollständig entladen werden.
- Nach dem Entladen sollten Bleibatterien so schnell wie möglich wieder aufgeladen werden.
- Bei Zyklischem Betrieb und mittleren Ladestäden ist eine regelmäßige Volladung sinnvoll.
- Die Lebensdauer steigt mit sinkender Temperatur. Ab -5°C kann allerdings das Elektrolyt einfrieren.
- Die Lagerung sollte immer im voll geladenen Zustand erfolgen. Eine regelmäßige Nachladung ist alle 3-6 Monate abhängig von der Lagertemperatur nötig.
Eigenschaften von Bleiakkus
Grundlegende Eigenschaften
- Zellspannung: ca. 2V
- theoretische Spezifische Energie: ca. 161 Wh/kg
- Verluste: (35% begrenzte Aktivmassenutzung, 14% Säureverdünnung, 13% Säureüberschuss, 14% Stromableiter, 5% Gehäuse etc.)
- praktische Spezifische Energie: ca. 35 Wh/kg
- Spezifische Leistung: 100-200 W/kg (kurzzeitig bis zu 1000 W/kg)
- Preis: ca. 50 €/kWh
Vorteile
- Hohe Zellspannung
- Hohe Sicherheit auch bei flascher Verwendung
- Hohe Lebensdauer möglich (insbesondere im Erhaltungsladungsbetrieb)
- Recycling einfach möglich
Nachteile
- geringe spezifische Energie
- geringe Zyklenfestigkeit
- schlechte Lagerfähigkeit
Anwendungsbereiche von Bleiakkus
- Traktionsanwendungen wie z.B. Gabelstapler (Blei-Antimon wegen guter Zyklenfestigekeit mit dem Nachteil der generellen Alterung)
- Starterbatterien
- USV-Batterien und Alarmanlagen (Erhaltungsladung)
